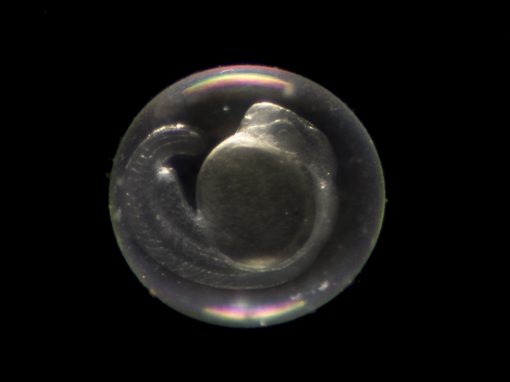
Des chercheurs de l’université de Pittsburgh ont mis au point un nouveau « modèle embryonnaire », dérivé de cellules adultes, « qui reproduit les principales caractéristiques du début du développement humain, notamment la production de cellules sanguines ». Ce nouveau « modèle », baptisé « Embryoïde-heX »[1] est décrit dans la revue Nature [2].
« Modéliser » les « premiers stades de la production de sang chez l’homme »
Les embryoïdes-heX ont formé des « structures similaires aux premiers sites de production de cellules sanguines », les îlots sanguins, indiquent les scientifiques. En outre, les chercheurs ont également détecté des progéniteurs de globules rouges, de plaquettes et de différents types de globules blancs.
« Nous avons pu modéliser quelque chose d’extrêmement similaire aux premiers stades de la production de sang chez l’homme », résume le Dr Mo Ebrahimkhani, professeur associé à l’université de Pittsburgh et auteur principal de l’étude. « La production de cellules sanguines est une avancée clé de ce modèle d’embryon qui fait progresser le domaine », affirme-t-il (cf. « Embryons de synthèse » humains : les annonces se multiplient).
Le recours aux iPS
Pour développer ces embryoïdes-heX, les chercheurs ont utilisé des cellules souches pluripotentes induites, générées à partir de cellules adultes. Ils les ont « programmées » avec un « circuit génétique » qui « dirige le développement précoce des tissus ». Ce circuit n’est activé que par une substance chimique appelée doxycycline.
Lorsque ces iPS modifiées sont mélangées in vitro avec des cellules iPS « standard » et induites par l’ajout de doxycycline, les cellules modifiées se développent et déclenchent l’organisation des iPS standard en « structures tridimensionnelles qui ressemblent à certaines caractéristiques d’un embryon ».
Ainsi, comme un embryon, les embryoïdes-heX sont dotés d’un tissu embryonnaire et d’une structure de sac vitellin. Le tissu reste « ancré » à la boîte de Petri au fur et à mesure de sa croissance, formant « une grande couche de sac vitellin » avec « des dizaines d’embryons côte à côte »[3].
« D’autres modèles ressemblant à des embryons n’ont permis qu’une différenciation très limitée du tissu du sac vitellin », indique le Dr Mo Ebrahimkhani.
Rassurer, encore
Les embryoïdes-heX ne contiennent pas de trophoblaste, et le sac vitellin est ouvert, non pas une cavité fermée. L’absence de ces caractéristiques les « empêche de devenir de véritables embryons ou d’avoir le potentiel d’être implantés pour se développer complètement », veulent rassurer les chercheurs (cf. Embryoïdes : l’ABM propose une « troisième voie » pour « encadrer » les recherches).
Les scientifiques vantent divers « avantages » de leurs embryoïdes par rapport à d’autres « modèles embryonnaires » : l’embryoïde-heX « s’auto-organise en se développant à partir d’une boîte de Petri bidimensionnelle », il utilise des milieux de croissance « standard » et il est « activé » par un seul produit chimique « au lieu de dépendre d’un cocktail complexe de facteurs de croissance qui peuvent être difficiles à répliquer ».
Selon Mo Ebrahimkhani, cette approche signifie que les embryoïdes-heX peuvent être « facilement stockés, expédiés et cultivés dans différents laboratoires avec un haut niveau d’efficacité ».
Parmi les potentielles applications envisagées, le chercheur envisage le développement de « meilleures méthodes de culture de cellules pour les transfusions sanguines, les nouvelles thérapies cellulaires et les greffes de cellules souches hématopoïétiques ».
[1] heX-Embryoid
[2] Joshua Hislop et al, Modeling post-implantation human development to yolk sac blood emergence, Nature (2023). DOI: 10.1038/s41586-023-06914-8
[3] « Au cours du développement embryonnaire normal, les cellules se segmentent en trois : le trophoblaste, qui deviendra le placenta, une couche de cellules extra-embryonnaires qui produit le sac vitellin, source de nutriments, et la couche embryonnaire qui donnera naissance à l’embryon lui-même et au sac amniotique qui protège l’embryon en développement ».
Source : Phys.org, University of Pittsburgh (13/12/2023)