Leur pluripotence
Un article récent du Journal of Experimental Medicine (1) confirme de façon étonnante les espoirs thérapeutiques des cellules souches contenues dans le sang de cordon ombilical. Initialement utilisées par le Dr. Eliane Gluckman pour les greffes hématologiques chez l’enfant (2) puis chez l’adulte (3), les cellules souches du cordon promettent de nombreuses applications extra-hématologiques pour des greffes cardiaques, vasculaires, osseuses, hépatiques et neuronales.
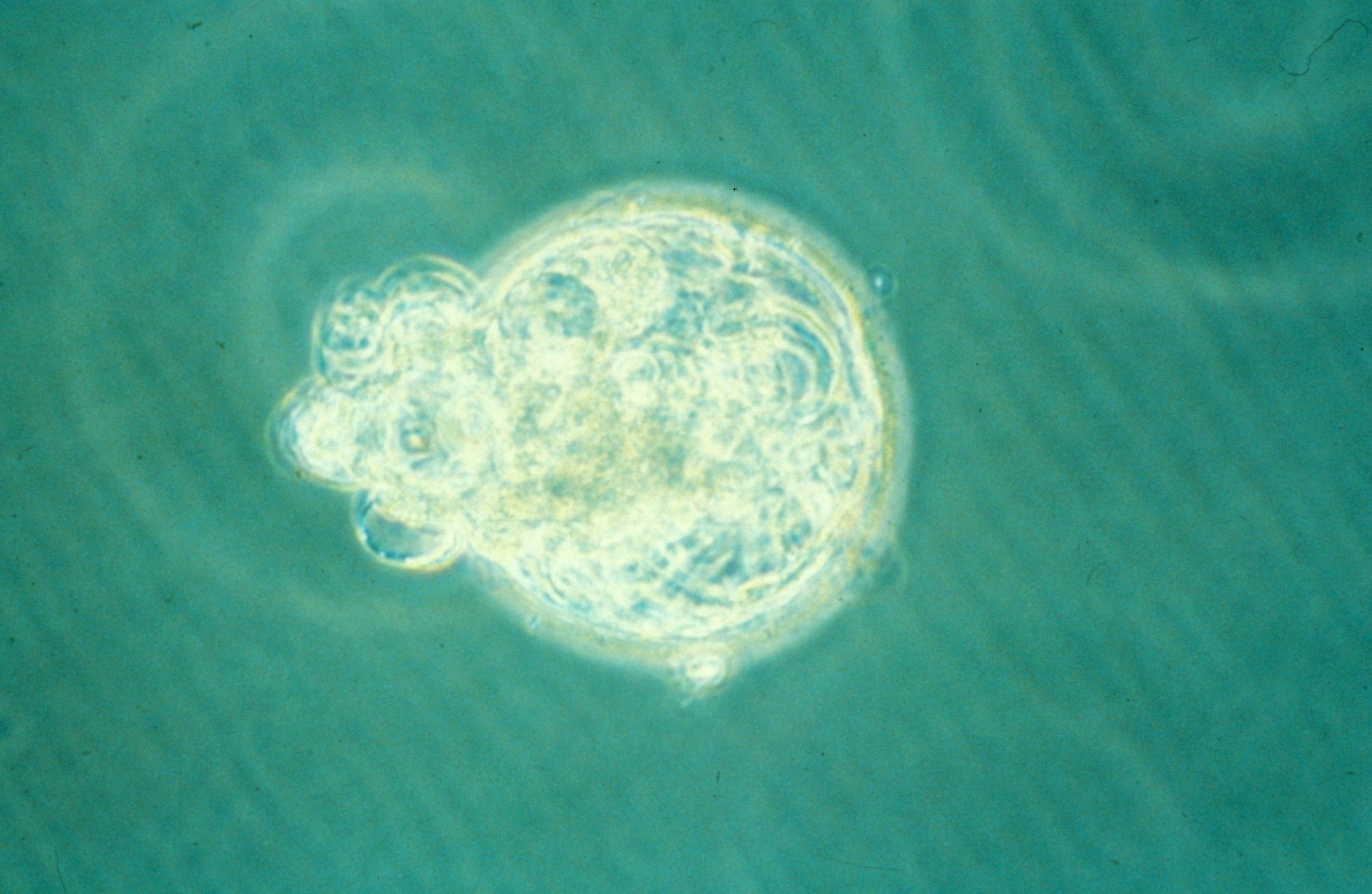
Collectées en faible quantité à la naissance, les cellules souches du sang de cordon ont pu être augmentées ex vivo sans perdre de leur pluripotence et se différencier en groupes homogènes d’adipocytes, hépatocytes, ostéoblastes, chondroblastes, cellules cardiaques et cellules neurales. Baptisées unrestricted somatic stem cells (USSCs), ces cellules souches placentaires sont parvenues à régénérer in vitro et in vivo de l’os, du cartilage, des cellules du foie, du cœur et des neurones. Moins quiescentes que les cellules souches adultes, leur plasticité se rapproche des cellules souches embryonnaires, avec l’avantage qu’elles n’induisent pas d’effet tumorigène après transplantation. L’équipe de la Düsseldorf Medical School conclue que le sang de cordon « pourrait ainsi servir de source universelle pour la thérapie cellulaire et la médecine régénérative » (J. Exp. Med., 2004 : 200, 2) et ce, sans recourir aux embryons humains, au clonage thérapeutique, ou aux bébés médicaments.
En effet, pourquoi donc fabriquer des clones embryonnaires alors qu’il existe des techniques alternatives, médicalement efficaces et éthiquement légitimes ? Encore discrètement évoqué dans le débat public sur les cellules souches embryonnaires et adultes, le sang de cordon pourrait représenter le point d’équilibre entre l’éthique et la clinique, c’est-à-dire la voie moyenne entre le respect de la vie humaine et le droit des malades à bénéficier des avancées de la médecine régénérative.
Enfant médicament /discrimination
Pourquoi créer des bébés médicaments par FIV, puis les sélectionner par Diagnostic pré-implantatoire (DPI) puisque, in fine, l’objectif visé consiste seulement à recueillir un sang de cordon histocompatible en vue d’une greffe ? Dans une situation d’urgence, pourquoi fabriquer sur mesure – et de façon si complexe – des donneurs sur pieds, alors qu’on pourrait recueillir le même greffon histocompatible sans délais de gestation, si les banques publiques de sang placentaire disposaient d’un nombre suffisant de typages HLA ?
Au-delà des importantes réserves concernant l’approche réifiante et utilitariste de l’enfant médicament, soulignons qu’au plan éthique, cette technique constitue une forme caractérisée de discrimination positive, dès lors que l’on sélectionne l’embryon par DPI sur le seul critère de son profil génétique. Or la Convention d’Oviedo et la Déclaration universelle sur le Génome humain se rejoignent expressément pour rappeler que « nul ne doit faire l’objet de discriminations fondées sur ses caractéristiques génétiques » (4).
Comment résoudre une telle contradiction ? En effet, l’existence de l’enfant médicament est suspendue à son génotype ; elle relève d’une discrimination positive fondée sur des caractéristiques génétiques. Légalisée en France par la loi du 4 août 2004, la création de bébés médicaments repose sur l’argument que, dans certaines conditions, la fin (obtenir un cordon histocompatible) justifierait les moyens (sélectionner un enfant selon son profil génétique).
La création précipitée d’un enfant médicament représente-t-elle vraiment la seule et unique option, celle de la dernière chance ? Pour atteindre le même objectif thérapeutique, l’élargissement des banques de sang de cordon constitue sans doute une alternative éthique, réaliste et durable.
Remplacer les banques de moelle
Il reste cependant à convaincre les gouvernements d’investir dans les banques publiques de sang placentaire afin d’augmenter le nombre d’unités cryopréservées, mutualiser les ressources biologiques à l’échelle mondiale et finalement, remédier progressivement à la pénurie chronique des banques d’organes. Aujourd’hui, il existe 170,000 unités de sang de cordon dans les 37 banques publiques pour couvrir les besoins de 6 milliards d’individus. Le Congrès américain a voté en 2004 un budget de $150 millions pour doter ses banques publiques de 150,000 unités en 5 ans, soit l’équivalent du nombre total d’unités de cordon dans le monde. L’objectif visé consisterait à remplacer progressivement les banques de moelle par des banques de sang de cordon. En effet, outre leur efficacité comparables pour les greffes hématologiques chez l’enfant et chez l’adulte (N. Eng. J. Med. 2004, 351 ; 22), la banque de sang de cordon offre des avantages inégalés comparés aux registres de moelle, car les greffons sont immédiatement disponibles, recueillis sans risque et conservables près de 20 ans.
Les banques de sang de cordon portent d’importantes promesses d’applications cliniques (cardiaques, hépatiques, osseuses, vasculaires, neuronales) dépassant largement les usages de la greffe de moelle. A l’instar des Etats-Unis, le Japon et l’Australie ont également choisi de privilégier leurs banques de sang de cordon plutôt que d’investir dans le recrutement de nouveaux donneurs de moelle. Paradoxalement, la France a récemment décidé d’adopter la politique inverse en élargissant le registre des donneurs de moelle de 100,000 unités d’ici 2015, tout en plafonnant le nombre de cordons à 5,000 unités pour 60 millions de français. Pionnière en 1988, la France occupe désormais le 14ème rang mondial en nombre d’unités de sang placentaire par habitant (5).
1 Kögler G, Sensken S, Airey J, et al., A New Human Somatic Stem Cell from Placental Cord Blood with Intrinsic Pluripotent Differentiation Potential, Journal of Experimental Medicine, 2004 ; 200, n°2: 123-135.
2 Gluckman E, Broxmeyer HA, Auerbach AD, et al., Hematopoietic reconstitution in a patient with Fanconi’s anemia by means of umbilical-cord blood from an HLA-identical sibling. N. Eng. J. Med. 1989 ; 321 : 1174-8.
3 Rocha V, Labopin M, Sanz G, et al., Transplants of Umbilical-Cord Blood or Bone Marrow from Unrelated Donors in Adults with Acute Leukemia, N. Eng. J. Med. 2004 ; 351: 2276-85. Voir aussi Laughlin M, Eapen M, Rubinstein P, et al., Outcomes after Transplantation of Cord Blood or Bone Marrow from Unrelated Donors in Adults with Leukemia, N. Eng. J. Med. 2004 ; 351: 2265-75.
4 Unesco, Déclaration universelle sur le génome humain et les droits de l’homme, 1997 : articles 2 et 6. Oviedo Convention on Human Rights and Biomedicine : article 11.
5 BMDW, Annual Report, 2004.